消化酵素ペプシンと胃の関係について見た後、おもむろにもう一つの代表的な消化酵素であるトリプシンについて、話に出すだけ出して時間切れにつき中途終了していたのが前回でした。
せっかくなのでそのトリプシンについてちょろっと触れてみようと思うのですが、まず、こちらは十二指腸~小腸で働くものだということで、強酸の胃とは打って変わって、これらの臓器はアルカリ性の腸液で満たされていることから、トリプシンが機能するpHもアルカリ性になっています。
したがって、例の自己分解の話ではあまり触れていなかったものの、これら消化酵素の純品を保存する際は、自己分解をより防ぐべく、胃で働くペプシンはアルカリ性の溶液に、腸で働くトリプシンは酸性の溶液中で保管するのが基本となっている形なんですね。
改めて、例えばペプシンの認識部位(=そこが攻撃されて、タンパク質が分解される部分)は「酸性アミノ酸-芳香族アミノ酸」という2連の並びであり、その部位はペプシンの表面にはあまり露出しないという工夫がなされている…なんて話だったわけですけど、そうはいっても高速で溶液内を飛び回っている大量の酵素に対して完全防備というわけではありませんから、タンパク質分解酵素自身もタンパク質ですし、どうしても自己分解は少しずつ起こってしまいます。
なので、少しでも分解を防ぐために、各酵素の得意条件ではない条件、具体的には低温で、かつペプシンならアルカリ性・トリプシンなら酸性の溶液中に保存するという工夫がされることが多い、って話になるわけですね。
ちなみに、(前回終わりにちょろっと書いていましたが)ペプシンの認識部位は上述の通り「酸性アミノ酸-芳香族アミノ酸」という2連続で、それぞれ全20アミノ酸中2種類・4種類存在しますからこの認識部位が登場する確率は2/20×4/20=1/50となる一方……
トリプシンの認識部位は「塩基性アミノ酸」で、(実際塩基性アミノ酸は他にもあるものの、この場合は)リシン・アルギニンの2種類になるため、2/20=10分の1の確率で「トリプシンによって切断される部分」が登場してくることになりますから、ペプシンよりもトリプシンの方が圧倒的に細かくタンパク質を消化可能になっています。
これはまぁ消化の流れからも当然といえ、タンパク質という巨大分子はいわば「胃で大まかに分解された後、腸でさらに細かく消化され、アミノ酸がちょっとつながった程度のペプチドの形で栄養として吸収される」という形になっているわけですね。
(ちなみに以前の記事のどこかで「ペプシンの他に、胃にある他の酵素も分解に関わるんですね」などと書いてしまっていた気がしますが、タンパク質分解酵素に限れば、胃に存在するのはペプシンだけだったので(他に、糖や脂質分解酵素はあれど)、それは語弊のある記述でした。
ただし、タンパク質という巨大な分子は酵素の力のみで切れるわけではなく、実は酸性条件に置くだけで「加水分解」という、水分子の力で例の「電子の授受が起こり結合がぶち切れる」という反応も起こるので(これは特定の配列にはよらず、概ねランダムに(とはいえ構造=水分子のアクセスのしやすさや、近傍に存在するアミノ酸の化学的性質にも依存しますが)起こるものになります)、「大雑把にざっくり分解される」ことには変わらない感じだといえましょう。
またちなみに、腸にはトリプシン以外にも複数のタンパク質分解酵素が存在しており、ここで種々の酵素の力によって本当に細かく寸断され、吸収されやすい形になる、という形ですね。)
…で、今回はトリプシンの話に入ろうと思っていたのですが、ちょうどその「アミノ酸の出現頻度」について、僕自身、ざっくりとしたイメージはあるものの具体的な数字を見たことはそういえばなかったため、実際どういう頻度になっているのか、今回はちょっくらそんなデータに当たってみようかと思います。
…と、その前にそもそもの20種類のアミノ酸ですが、ちょうどこないだも書いていた通り、完全保留状態になっている「分子生物学入門」シリーズの記事で、激甘タンパク質ソーマチンの話からもうちょいでシリーズ最後のアミノ酸・タンパク質の構造の話に入る予定で、アミノ酸についてはその時に触れようと思っていたのですが、今回せっかくなので名前と(略記表記の)覚え方だけ紹介してみるといたしましょう。
まず、タンパク質はアミノ酸がつながってできたものですが、タンパク質はもちろん、そのアミノ酸も有機化合物なので、炭素原子が基本になっています。
炭素には4本の腕があり、アミノ酸を形成するその4本の腕の内、3本には必ず「水素」「アミノ基」「カルボキシ基」がくっついており…
(こないだの記事でもちょっと登場していましたが、アミノ基とカルボキシ基が手をつないでつながっていく形で、「アミノ→カルボ」という順番も形成されます)
…残り1つの腕、「側鎖」と呼ばれますが名前はともかく、そこに何がつながるかでアミノ酸が決定する感じなんですね。
まぁ今回は名前の紹介だけで、詳しい構造には触れないものの、せっかくですしちょっとだけ見ておくと、まず一番簡単なグリシンは側鎖が水素原子のみで、これが一番小さくて単純なアミノ酸になります。
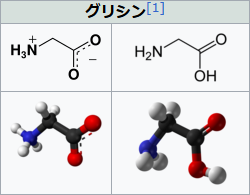
ずっと昔の「楽しい有機化学講座」でも触れていた話再び…ですが、上記の構造式では「炭素原子」と「炭素につながった水素」は省略して描かれることが多いので、これだと若干分かりづらいかもしれませんね。
より分かりやすい構造が、パッと検索したら脳科学辞典に掲載されていたので、こちらをお借りしましょう。
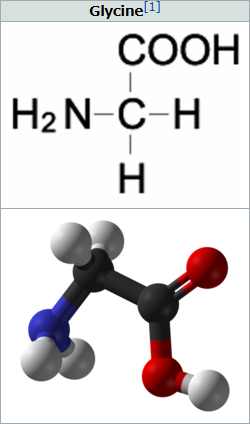
こちらは逆にカルボキシ基-COOHの二重結合とかが省略されていますが、アミノ酸の構造を知る上では、確実にこちらの方が分かりやすいですね。
不慣れな場合、全く別物に見えると思いますが、こちらは先ほどのWikipediaグリシンと全く同じものを描いている構造式になっています。
次に簡単なものは、有機化合物ではやはり「炭素」がくっついたものになりますから、炭素が1つ増えた側鎖=1本の腕はその中心の炭素原子とつないで、残りの3本には水素がついた、「-CH3」(メチル基)がつながったものが、二番目に単純なアラニンになります。
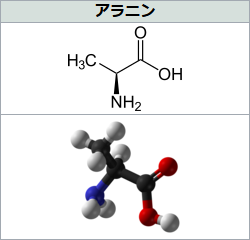
先ほどと同じく、(末端以外の)炭素省略図ではかなり分かりにくいので、略さず描いている丁寧な構造式は……なぜか脳科学辞典にはグリシンしかなかったので、こちらは検索したら出てきたコトバンクの記事からお借りしましょう(まぁこんなもんぐらい自分で描けよ、って話ですが(笑))。
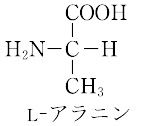
先ほどグリシンでは「H」だった、下にある「側鎖」が、こちらはCH3になったことがお分かりいただけると思います。
そんな感じで、まずは側鎖に「ただの炭素と水素がくっついただけ」という、何の特徴もないつまらんアミノ酸(まぁつまらなくはなく、重要なアミノ酸ですけどね(笑)。側鎖の炭素の数が違う(増えていく)だけです)から見てみると…
以下、日本語名(これも、カタカナなので表記揺れがあるものの、まぁ一番呼ばれがちな名前を掲載します)と、3文字表記・1文字表記の順に並べてみます。
1. グリシン:Gly、G
2. アラニン:Ala、A
3. バリン:Val、V
4. ロイシン:Leu、L
5. イソロイシン:Ile、I
続いて、側鎖に炭素&水素だけではなく、もうちょびっつだけ発展して、-OH基がくっついたものも並べちゃいましょう。
6. セリン:Ser、S
7. スレオニン:Thr、T
(個人的には「スレオニン」呼びを好みますが、文字表記の上では「トレオニン」の方が誤解がないかもしれませんね)
正直これも、化学的にはあんまり大きな特徴がない感じの、「平凡なアミノ酸」って感じですね。
さらには、ここからはかなり特徴があるといえる、側鎖に硫黄のSが付いたものも、「略式表記が分かりやすいシリーズ」で並べておきましょうか。
8. メチオニン:Met、M
9. システイン:Cys、C
硫黄原子はタンパク質を形成する上で極めて意味のあるものですが、まぁ今回構造や性質に深入りするのはやめておきましょう。
以上でおおよそ半分が出てきましたが、ここまでの3文字/1文字表記は、「分かりやすいシリーズ」と書いた通り大変素直で覚えやすいものであり、アミノ酸の名前さえ覚えていればほぼそのまんま書けばいいだけのやつなので、特記すべきものもない感じです。
(もちろん、大前提として、20種類のアミノ酸を覚えている必要はあるわけですが。)
唯一、ロイシンは「Leucine」なので(カタカナ読みだけからだと)ややこしいですけど、これは英語の場合「ルーシン」と言われますし、イソロイシンは名前そのまんま、ロイシンの兄弟分子(配置が換わっただけで、炭素の数はロイシンと全く同じ)なので、Iso-という接頭辞が付いただけであり、Leuに「I」がついてIleと覚えればまぁ間違いようがないといえましょう。
(正直「Iso」の方が日本人的には分かりやすいもんですが、「iso」自体は普通に英語の接頭辞なので紛らわしすぎますから、「アミノ酸のことである」と示すためにそれは避けられたのかな、って気がします。)
では続いて、こないだ最初に出てきた「酸性アミノ酸」と、それからその兄弟分子的なものをそれぞれ、まとめて見ていきましょう。
11. グルタミン酸:Glu、E
12. アスパラギン:Asn、N
13. グルタミン:Gln、Q
これらは、「A」も「G」も既にアラニンとグリシンというショボいアミノ酸に使われているので、特別な一文字表記を覚えねばいけない厄介なやつらですね。
かなり強引ですが、僕は学生時代にネットで見て「うむ、それは覚えやすい!」と思って記憶した覚え方が未だに根っこになっているので、それを紹介してみましょう。
まず、「酸」のないやつらはそもそも「酸」付きのやつそれぞれが中和された、いわば塩(えん)のフォームといえるんですけど、その中和型の一文字表記は「NQ」と、まぁ正直何の意味も根拠もないですが、何となく中性っぽい文字(Nはニュートラルだし、Qは何かアルファベット的に偏りがないというか他の文字との反応性がないというか、中性っぽい気がします。ちょっと無理がありますが(笑))で、セットでもう「酸性アミノ酸の中和型は、NQ!」と覚える感じです(笑)。
ただ、補足としてド忘れ防止の策がありまして、↓で触れる酸性アミノ酸もそうなのですが「アスパラギン」と「グルタミン」の頭文字はそれぞれAとGですけど、NQのアルファベットはその順番(A→G)で出てくる(よって、アルファベット順先のアスパラギンがN)、というのと…
さらに日本人限定のナイス覚え方として、グルタミン=Glnは「グルン」というQの文字の書き方そのものだということで、これは3文字表記含めかなり覚えやすくなっているような気がします。
そして、その3文字表記の方は、どちらも「ニュートラル=中和」な「n」で終わっていると覚えればOKといえましょう。
一方の酸性アミノ酸は、3文字表記はどちらも「n」ではなく、そのアミノ酸の名前そのまんまの素直な表記であり(Aspラギン酸とGluタミン酸)、1文字表記はもう全く何の根拠もないものの、これも先ほど同様「酸性アミノ酸は、DE!」と、横並びの2文字であるのも覚えやすいため、強引に「酸性はDE!」と覚える感じですね(笑)。
幸い、先ほど書いたとおり、A→GとD→Eの並び順は一致しているため、どちらがどちらかは名前さえ覚えていればすぐに思い出せる感じになっています。
(一応、酸を表す「aciD(アシッド)」の「D」で、「E」はまさに酸性アミノ酸のセットでその次の文字が使われた、という歴史だったと思いますけど、そんな御託はともかく、もう「酸性はDE」ですね(笑))
では続いて塩基性アミノ酸になりますが、こちらはトリプシンの所で書いた通り、リシンとアルギニンと、それからヒスチジンも「水に溶けてアルカリ性を示すアミノ酸」となるのですが(要は、代表的なアルカリ性物質であるアンモニアっぽい「-NH2」というアミノ基が、「必ず1つある」部分の他に、側鎖にも追加で存在するから塩基性になる感じです)、ヒスチジンはリング構造も持つため(厳密にはベンゼン環ではないものの、それに近いもので、Wikipediaの「芳香族アミノ酸」としても挙げられていました)、複数の特徴を備えたオシャレなアミノ酸といえますね。
今回は、話に挙がっていたトリプシンが認識するのもリシンとアルギニンだけですし、とりあえずその2つだけを挙げてみるとしましょう(その2つは覚えにくいので)。
14. アルギニン:Arg、R
15. リシン:Lys、K
アルギニンは、三文字表記のArgは素直なものの、「A」は例によって雑魚アミノ酸であるアラニンに取られてしまってますから、2文字目のRが使われる感じですね。
でもこれは、「Rギニン(アールギニン)」と考えれば、非常に覚えやすいものだといえましょう。
一方のリシンがKは……これはもう全く何の意味も語呂もなく、実際はLはロイシンで使われているため無理、2文字目のYも(まだ出てきてませんが)、3文字目のSも使われているという可哀想な分子につき、「Lの1つ前のKが割り当てられた」という形だったと思いますけど……
…これはもう、野球の三振を「K」で表すように(まぁこれは「ノックアウト」という意味はあるものの、ほとんどの小学生はそんなこと知らずに覚えていると思います(笑))、全く意味も関連付けもないけど「リシンはKだ」と、そういえばこれだけはまさに「いつの間にか覚えてしまった」の例でしかないですね。
まぁ、1つぐらいそういうのがいてもいいでしょう(笑)。
(…って、正直酸性シリーズもそれに近いものがありましたが(笑))
では最後に、芳香族アミノ酸4種、および芳香族ではないもののリング構造を持つ、正直一番仲間ハズレなやつ(他のアミノ酸と上手く結合したり並んだりすることができず、こいつがいると構造が崩れがちな、変なキモいやつ)も一緒に見ておきましょう。
16. フェニルアラニン:Phe、F
17. ヒスチジン:His、H
18. チロシン:Tyr、Y
19. トリプトファン:Trp、W
20. プロリン:Pro、P
そもそも芳香族といわれても何のこっちゃかもですが、これは例の六角形リングの、「いかにも有機化学」なあの構造を含むやつを呼ぶものでした。
で、ヒスチジンはベンゼン環そのものではないものの芳香環の仲間をもつので芳香族アミノ酸であり、しかも塩基性アミノ酸でもあるというのは上述の通りで、最後のプロリンはいびつなリングを持つだけで芳香族アミノ酸ではない、というのも今しがた先ほどチラッと書いていた通りです。
まぁ今回はグループ分けや構造の話ではないので深入りしないとして、覚え方は、特徴あるヒスチジンと仲間ハズレなそのカスアミノ酸であるプロリンは略式表記的には大変素直で覚えやすく、こいつらはそのまんまですね(His, H、Pro, P)。
また、チロシンも、Tがスレオニンに使われているので二文字目(tYr)を使ってYというのも、日本語読みだとちょっと悩ましい気もするものの、英語だと「タイロシン」なのでその英語呼び含めて覚えてもいいやつかもしれません。
そしてフェニルアラニンは、三文字表記はそのまんまPheで、一文字表記のPはプロリンに先を越されたため、これは音の近い「F」が採用されたということで、これは案外まぁ覚えやすい気がします(むしろ、「フェニル」も分かりやすく「Fenyl」であって欲しかった(笑))。
(なお、ベンゼン環が官能基(=炭素の腕と手をつなげる、1本腕の余った状態のもの)として使われる際は「フェニル基」と呼ばれる…というのは例の有機化学講座で何度か書いていたのですが(例:↓など)…
…まさにこの「フェニルアラニン」は、「アラニン」に「フェニル基=ベンゼン環」がついたものになるため、有機化学の知識があったら名前から構造式を描くのも容易いという感じになっているものですね(アラニンが2番目に単純なやつ=側鎖にメチル基がついただけ、ってのは常識なので)。)
そして最後トリプトファンは、Trpでこれも3文字全部別のやつに使われてしまっているため、苦肉の策で「トリプトファン」とは全く何の関係もない「W」が割り当てられた形ですが…
トリプトファンは前回触れていた通り一番大きなアミノ酸なので、何となく一番大きいアルファベットである「W」(別にそんな印象もないかもしれませんが、僕は「アミノ酸の覚え方」記事でそう書かれていて、「確かにね」と納得いきました(笑))である……と、これはアミノ酸のトリを飾る感じでまぁそういう覚え方もありかな、って気がします。
といった所で、今回唐突にアミノ酸の略号メインにそれぞれ触れてみました。
正直、当初考えていたより余裕で時間を食いまくったため、初稿アップには間に合わず追記で仕上げた形でしたが、そもそも正直こんなもん覚えても健康食品プロテインに詳しくなるとかそんなこともなく、ガチで何の意味もないんですけどね(笑)……
まぁ生命科学・生化学系の学生は覚えるのが必須(というか、あまりにも出て来すぎるので、正直いつの間にか覚えてるわけですが)であり、僕は最初大体こんな感じで覚えました、という紹介程度の話でした。
本当は各アミノ酸の出現頻度を見ようと思っていたのですが余裕で完全に間に合わなかったので、次回持ち越しとさせていただきましょう。