原子に関するベーシックな話を一通り見終えて、ご質問の方に触れていくターンに入っていました。
早速、アンさんよりいただいていたご質問の続きに参りましょう。
毎度大変素晴らしい着眼点からの面白いポイント、感謝感激雨霰にございます…!
水でない液体(例えばエタノール?)の場合も、pHがあって、水素イオンが存在して、その水素イオンの量によって酸性とアルカリ性があって…ということなんですよね?
水素イオンでない陽イオンが存在する液体というのもあるとしたら、そこにはpHや酸性アルカリ性というものは( pHが水素パワーなら当然水素イオンでなければpHとは言わないと思われるので)無いとして、それらに変わるものっていうのは何かあるんですかね?
イオンの中でも水素は特別ですか?
なんて、ちょっと思いついたことを投げましたが、恐らくそれを解説していただいたとしても、ちゃんと理解できるとも思えないので、「あぁ、それはちがいまーす」くらいの感じで大丈夫です笑
⇒これまたナイスポイントですねぇ~。
もちろん、エタノールの場合も然りで、液体の中で自発的にH+が発生することがあるのなら、pHの計測は可能になります。
とはいえ、逆にいえばpHというのは、H+=水素イオン濃度のことに他なりませんから、H+が発生し得ない液体にpHという概念は存在しませんし、さらにいえば、以前エタノールのpHを見ていた際(↓)にも書いていた通り…
この「エタノールのpH」というのはあくまで「エタノール視点のpH」であり(何のこっちゃですが、上記記事で書いてたような話=水素イオンと、エトキシドイオンとの関係を見たものですね)、これは水のpH、つまりH+とOH-の関係を述べた、汎用されているいわゆる「pH」(両者の濃度をかけたら、10-14になる、という例のあれ)とは全然関係ないものになっている、ともいえますね。
「水素イオンの発生し得ない液体」って何かあるかな…?とちょっと考えましたが、有機物は基本的に何だかんだ水素が顔を出してきますし(炭素の余った腕には、基本水素がいるので)、案外パッと浮かびませんでしたけど、まぁ裏技的に、常温で液体である唯一の金属・水銀先生の力をお借りしましょうか。
水銀は液体ですけど、言うまでもなく水銀原子のみからなる金属なので、(元素記号はHgなので、パッと見だとHはいそうですけど(笑))金属は陽イオンになりやすい物質ですし、ここに同じく陽イオンになりやすい水素の入り込む余地は一切ないといえますね(せめて陰イオンなら、陽イオンになった水銀とくっつくこともあるかもしれませんが)。
厚労省の安全データシート(↓)を見てみると…
ちゃんと、↓のように…
9.物理的及び化学的性質 物理的状態 形状 液体(Merck (14th, 2006) ) 色 銀色(Sax (11th, 2004)) 臭い 無臭(HSDB (2010)) 臭いのしきい(閾)値 データなし。 pH データなし。
「pH データなし。」となっていますね!
そんなわけで、pHという概念すら存在しない液体もありますし、むしろ「酸性・アルカリ性」ってのは水の中での話ですから、例のエタノールのpHのように、pHという概念はあっても中性がpH 7ではないなど、そもそもあんまり考える意味のない数字になっていると言えるように思います。
(もちろん、「エタノールを水に溶かした際、pHがどう動くか?」みたいな話はありますし、例えば同じ有機物であるフェノールは、水に溶かすと水素イオンを放出するため、これは「酸性物質である」などといわれますけれども、これもあくまでいわば「水視点のpH」を考えている感じですね。)
若干ややこしいですが次の関連質問に移りますと、「水素イオンでない陽イオンが存在する液体というのもあるとしたら、そこにはpHや酸性アルカリ性というものは無いとして、それらに変わるものっていうのは何かあるんですかね?」というポイントですが、これもズバリ、基本的に液体の王者は水であるため、水以外での挙動を考える意味があまりありませんから、その分子がイオンになったものも考える意味が皆無であり、特にそういうデータはまとめられていないように思います。
(もちろん計測すればその液体から発生する陽イオンと陰イオン濃度の掛け算がいくつになるか?…とかは求まるものの、広く必要とされるデータではない、ってことですね。)
あぁ、先ほどは「水素イオンのない液体、パッと浮かびませんが…」と書きましたけど、よぉ考えたら普通に、普段実験とかでめっちゃ使ってる有機溶媒の中に沢山あることに気が付きました!
いわゆる「非プロトン性溶媒」と呼ばれるやつで…
↑のウィ記事に表がまとめられていましたね。
(ちなみに「プロトン」は「陽子」の英語であり、水素イオンは陽子そのものでしたから、水素イオンのことはしばしば(日本語でも)「プロトン」と呼ばれます)
非プロトン性溶媒の部分を抜粋させていただくと…
溶媒 化学式 沸点 誘電率 密度 結合双極子モーメント (D) 非プロトン性極性溶媒 N-メチルピロリドン CH3NC(O)C3H6 202 ℃ 32.2 1.028 g/mL 4.1 D ジクロロメタン (DCM) CH2Cl2 40 ℃ 9.1 1.3266 g/mL 1.60 D テトラヒドロフラン (THF) C4H8O 66 ℃ 7.5 0.886 g/mL 1.75 D 酢酸エチル (EtOAc) CH3CO2CH2CH3 77 ℃ 6.0 0.894 g/mL 1.78 D アセトン CH3C(O)CH3 56 ℃ 21 0.786 g/mL 2.88 D ジメチルホルムアミド (DMF) HC(O)N(CH3)2 153 ℃ 38 0.944 g/mL 3.82 D アセトニトリル (MeCN) CH3CN 82 ℃ 37 0.786 g/mL 3.92 D ジメチルスルホキシド (DMSO) CH3S(O)CH3 189 ℃ 47 1.092 g/mL 3.96 D 炭酸プロピレン (PC) C4H6O3 242 ℃ 64 1.205 g/mL 4.90 D プロトン性極性溶媒 ギ酸 HCO2H 101 ℃ 58 1.21 g/mL 1.41 D n-ブタノール CH3CH2CH2CH2OH 118 ℃ 18 0.810 g/mL 1.63 D イソプロパノール (IPA) (CH3)2CH(OH) 82 ℃ 18 0.785 g/mL 1.66 D ニトロメタン CH3NO2 100–103 ℃ 35.87 1.1371 g/mL 3.56 D エタノール (EtOH) CH3CH2OH 79 ℃ 24.55 0.789 g/mL 1.69 D メタノール (MeOH) CH3OH 65 ℃ 33 0.791 g/mL 1.70 D 酢酸 (AcOH) CH3-CO2H 118 ℃ 6.2 1.049 g/mL 1.74 D 水 H2O 100 ℃ 80 1.000 g/mL 1.85 D
ジメチルスルホキシド、日本語でも英語でも略してDMSOと呼ばれますが(日本語では「ジムソ」とか「ディムソ」とか呼ばれることも多いものの、英語ならやっぱりアルファベットべた読みの「ディーエムエスォー」って感じですね)、これは、水に溶けにくい有機物を溶かすために非常によく使われる溶媒、いわば「有機物版の水」ともいえる基本的な王道液体なんですが、こいつはそういえば(分子内にHはいるものの)水素イオンは決して放出しないやつでしたね!
他に画像がなかったので無理やり、アイキャッチ画像用にDMSOのウィキP画像をお借りさせていただきましょう。
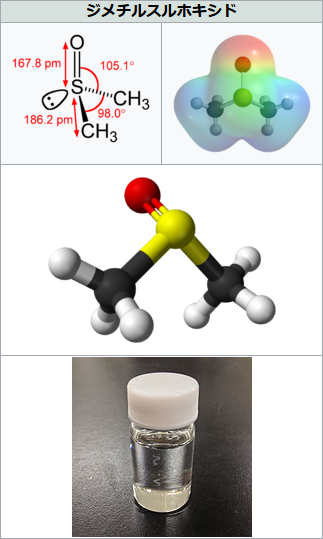
こいつは画像にもある通り液体ですが、融点は19℃という微妙にかつ絶妙に高い所にあり、ちょっと氷の上に置いてしまったり、冷蔵庫の中に置いただけ…どころか周りの気温が低くなりすぎただけで一瞬で凍ってしまうという、ウザイやつなのです(笑)。
まぁ、逆にその性質がありがたいこともあるわけですが、こちらは生命科学系でも多用する液体といえましょう。
他にも、「アセトン」とかは日常的にもどっかで聞いたことがあるのではないかと思いますが、いずれにせよ、表には「化学式」「沸点」「誘電率」「密度」「結合双極子モーメント」なるデータがあるものの、当たり前ですが液体のくせに「pH」というデータは存在しないんですね!
双極子モーメントは大学の電磁気学で習った気もしますが、無視した方がいいのは↓の記事をご覧いただければ納得いただけることでしょう(笑)。
クソムズ数式連発すぎ、ワロタ(笑)。
一応ごく簡単に書けばこれは分子内の電荷の偏りを表す数字で、これが大きいほど分子内に電気の偏りがある=イオンになりやすいといえるものの、まぁそれ以上詳しいことは僕にも分かりません(笑)。
こんなどうでも良すぎる値があるのにpHは出てこない時点で、この表においてpHは無意味なものであることの裏返しといえそうですね。
(もちろん、エタノールや水は、下半分、「プロトン性の溶媒」となっており、こいつらはギ酸や酢酸が酸性物質など、水溶液のpHがどうなるか、多少意味のあるデータにはなりますが…)
…といった話を踏まえ、また、まさにちょうど前回も似たようなことを書いていた通り、この段落最後のご質問、「イオンの中でも水素は特別ですか?」は、正直極めて特別な存在だといえるように思います。
もちろん地球を地球たらしめている分子、水の核を成す原子であることもそうですが、原子番号1=陽子1つと電子1つという簡潔極まりないものから成るというのも、水素の特別さに拍車をかけている感じですね。
では次回も続きのご質問に触れていこうと思います。